Синдром микробной контаминации тонкой кишки. Синдром избыточного бактериального роста в кишечнике: что это такое, лечение, симптомы, причины, признаки
Вследствие бактерицидного действия соляной кислоты желудка и перемещения содержимого по тонкой кишке в результате перистальтики проксимальные отделы тонкой кишки в нормальных условиях содержат относительно малое количество бактерий, в основном это грам-положительные микроорганизмы и анаэробы из полости рта. В подвздошной кишке количество микрофлоры возрастает до 109колониеобразующих единиц (КОЕ)/мл за счет грам-отрицательных микроорганизмов и анаэробов. И, наконец, в толстой кишке появляется огромное количество бактериальных тел, в основном анаэробов, при концентрации 10"2 КОЕ/мл.
Избыточная пролиферация бактерий в тонкой кишке (ИПБТК) характеризуется появлением большого количества бактерий в тонкой кишке из числа тех, что в норме заселяют в основном толстую кишку. Традиционно об ИПБТК говорят, если в посеве аспирата, взятого на уровне проксимального отдела тонкой кишки, обнаруживается более 105 КОЕ/мл. Недавно предложено пересмотреть определение и понизить пороговый уровень до 103-104 КОЕ/ мл бактерий толстокишечного типа при сочетании этого показателя с характерными симптомами. ИПБТК сейчас все чаще признают причиной мальабсорбции. Есть мнение, что избыточный рост бактерий лежит в основе многих недовыясненных причин различных неспецифических желудочно-кишечных расстройств.
Эпидемиология
Распространенность ИПБТК и ее отношение к ряду клинических состояний пока не уточнены, так как существуют разночтения, которые касаются как самого понятия ИПБТК, так и методов выявления. Более того, набор клинических симптомов при ИПБТК во многом перекликается с проявлениями многих других желудочно-кишечных расстройств.
Высокая степень настороженности должна сохраняться в отношении больных с фоновыми болезнями, разрушающими защитные барьеры, которые существуют в норме и предотвращают ИПБТК. Показатель распространенности ИПБТК меняется в зависимости от характеристик исследуемой популяции и используемого метода диагностики. Так, при проведении дыхательного теста с с глюкозой у взрослых испытуемых ИПБТК выявляют в 0-12% случаев, а при аналогичной пробе с лактулозой - в 22%. Как оказалось, ИПБТК имеет большее распространение среди пожилых людей. У новорожденных и пожилых ИПБТК может вести к тяжелым состояниям и даже смертельному исходу, однако точных показателей летальности, непосредственно связанных с ИПБТК, нигде не приводится.
Патогенез
К наиболее важным факторам в патогенезе ИПБТК относят нарушения двигательной функции кишечника, изменения анатомии ЖКТ, способствующие застою содержимого (большие дуоденальные дивертикулы, наложенные хирургические анастомозы, резекция зоны илеоцекального клапана), ослабление выработки соляной кислоты желудком, пожилой возраст. Хоть и в меньшей степени, но защищают от ИПБТК и желчь, и протеолитические панкреатические ферменты, и внутренняя иммунная система. Тем не менее выявить предрасполагающий фактор не всегда легко. ИПБТК может развиваться как при наличии специфического патогенетического механизма (например, при сахарном диабете, синдроме слепой петли, гастрэктомии, иммунодефицитных состояниях), так и благодаря комбинации перечисленных выше факторов. Например, хроническому панкреатиту сопутствуют ослабление моторики кишечника и снижение выработки панкреатических ферментов; ожирению свойственно сочетание с изменением микрофлоры кишечника и нарушениями двигательной функции тонкой кишки; цирроз печени и неалкогольный стеатогепатит обусловливают гипомоторику кишок и усиление проницаемости кишечной стенки.
Симптомы и признаки
Первоначально ИПБТК считали состоянием, неизменно провоцирующим диарею, пониженное питание, авитаминозы и снижение массы тела, и все это на фоне условий, которые способствуют стагнации кишечного содержимого, однако «классическая картина» болезни сейчас встречается редко. Характерно, что больные с ИПБТК почти всегда предъявляют совершенно неспецифические жалобы, такие как боль в животе и дискомфорт, повышенное отхождение газов, вздутие живота, изменение частоты стула при отсутствии явных факторов, предрасполагающих к этому. У детей с ИПБТК могут отмечаться диарея и боль в животе, в то время как нарушение питания и авитаминозы обычно не развиваются. Напротив, у пожилых больных ИПБТК может ничем себя не проявлять или выражаться в необъяснимом похудении и мальабсорбции. Клиническая картина ИПБТК может развиваться по различным сценариям, среди которых, чрезмерное газообразование, индукция диареи, нарушение всасывания и т.п.
Патогенез клинических проявлений у больных с избыточной пролиферацией бактерий в тонкой кишке
- Ферментация углеводов кишечными бактериями ведет к выработке диоксида углерода, водорода и метана, которые вызывают вздутие и растяжение живота, абдоминальную боль и избыточное отхождение газов
- Короткоцепочечные жирные кислоты, образуемые в процессе ферментации, стимулируют секрецию воды и электролитов, что приводит к диарее
- Деконъюгация солей желчных кислот может приводить к мальабсорбции жиров, стреаторее, снижению массы тела и гиповитаминозу за счет жирорастворимых витаминов A, D, Е и К
- Потребление витамина В 12 кишечными микроорганизмами может привести к макроцитарной анемии и неврологическим расстройствам
- Разрушение щеточной каймы энтероцитов нарушает усвоение углеводов и белков, хотя, при ИПБТК это наблюдается очень редко
Факты, подтверждающие взаимосвязь между избыточной пролиферацией бактерий в тонкой кишке и синдромом раздраженного кишечника
- Усиленная ферментация и повышенное содержание газа в тонкой кишке у больных с СРК по сравнению с контролем
- Избыточное количество бактерий толстокишечного типа в проксимальном отделе тонкой кишки у больных с СРК
- В отличие от контроля, не соответствующие норме результаты дыхательных тестов у больных с СРК
- Образование водорода наблюдают у больных, страдающих СРК с диареей; «метанообразователи» - пациенты с СРК со склонностью к запорам
- Лечение антибиотиками купирует симптоматику СРК, соответственно приходят к норме и дыхательные тесты
- В одном из контролируемых исследований после лечения антибиотиками наблюдали хороший результат, который сохранялся как минимум 12 нед
- Есть модель на животных, которая соединяет воедино теорию становления ИПБТК с постинфекционным СРК. Изменение стула на фоне ИПБТК и уменьшение количества ИСКК в глубоком мышечном сплетении по прошествии значительного времени после острой инфекции, вызванной С. jejuni, наблюдали у грызунов.
Хотя ИПБТК традиционно связывали с диареей и мальабсорбцией, на сегодняшний день накоплены свидетельства, которые позволяют вменить ИПБТК также развитие заболеваний без патогномоничных биохимических, иммунологических и/или гистологических характеристик. Действительно, в течение последнего десятилетия накоплена масса данных в поддержку роли ИПБТК в развитии СРК. Первоначальная противоречивость мнений в отношении роли ИПБТК в становлении СРК порождалась малой точностью дыхательных тестов в качестве способа диагностики ИПБТК. Последний метод, действительно, рассматривается в качестве диагностического «золотого стандарта», однако в одном из последних систематических литературных обзоров авторы все же показали, что пока ни один из тестов не приобрел достаточной доказательной базы для его надежного использования в диагностике ИПБТК.
Диагностика
Симптомокомплекс в виде диареи, снижения массы тела, вздутия живота и повышенного отхождения газов у больного с факторами риска ИПБТК, независимо от того, есть мальабсорбция или ее нет, должен заставить клинициста подумать о проведении лабораторного анализа для выявления избыточной пролиферации бактерий, особенно если больной не ответил на проводимую до этого эмпирическую терапию. Скорее всего, у больных без предрасполагающих факторов из-за неспецифичности симптомов ИПБТК часто пропускают. При отсутствии «золотого стандарта» наиболее практичный метод выявления ИПБТК состоит в следующем: подход «пролечи и смотри результат» в сочетании с дыхательным тестом для того, чтобы можно было выделить тех больных, которым особенно показана антибиотикотерапия; при этом дыхательный тест должен нормализоваться после лечения.
Посев аспирата из проксимального отдела тонкой кишки
Посев с подсчетом количества бактерий в содержимом проксимального отдела тонкой кишки признан «золотым стандартом» для диагностики ИПБТК. Результат соответствует патологии при обнаружении более 105 КОЕ/мл. Не так давно предложили более низкий уровень - более 103 КОЕ/мл микробов толстокишечного типа при наличии соответствующей клинической картины. Посев аспирата из проксимального отдела тонкой кишки, однако, имеет много ограничений, которые ставят под сомнение чувствительность метода. Диагностика таким способом признается довольно инвазивной и дорогостоящей процедурой, требующей эндоскопии; последняя, в свою очередь, допускает ситуацию, когда аспират может быть заражен микрофлорой из полости рта. При выполнении ЭГДС, кроме того, удается достичь только двенадцатиперстной кишки, но посев материала с этого уровня может привести к недооценке избыточной бактериальной пролиферации в более дистальных отделах кишечника. К тому же ИПБТК может быть неравномерной по всей длине тонкой кишки, развиваясь лишь в отдельных зонах («пятнистое» распределение), что еще больше понижает значение посевов аспирата. Дополнительный нюанс состоит в том, что трудно работать с образцом аспирата для посева анаэробов: весьма реальны ложноотрицательные результаты, когда аспират, прежде чем попасть в питательную среду для роста, успевает проконтактировать с кислородом. И, наконец, используя молекулярные методики, выяснили, что обычными культуральными методами можно идентифицировать только 40% общей микрофлоры кишечника.
Дыхательные тесты
Дыхательные тесты/пробы основаны на принципе ферментации углеводного субстрата просветными бактериями, что ведет к дополнительному образованию газа (водорода или метана), его всасыванию и в конечном итоге выведению с выдыхаемым воздухом. Дыхательные тесты безопасны, неинвазивны и легковыполнимы. Среди них особенно популярен водородный тест. Его проводят после пробного завтрака с глюкозой или лактулозой. Другие дыхательные тесты для выявления ИПБТК (тест с желчными кислотами и ксилозой, меченной 14С) доступны не столь широко, поэтому их значение для диагностики ИПБТК не установлено.
Для проведения дыхательных тестов имеется ряд ограничений. Для того чтобы быть уверенным в точности водородного дыхательного теста, углевод-содержащий раствор должен быть использован не позже чем через 12 ч после приготовления. Перед выполнением пробы необходимо прополоскать рот антисептическим раствором. Сразу же проводят анализ и определяют концентрацию метана в выдыхаемом воздухе. Это требуется, чтобы избежать ложноотрицательных результатов из-за возможного присутствия во рту метанобразующих бактерий, способных трансформировать водород в метан.
Во время тестирования, которое назначают после ночного периода голодания, делают забор исходного образца выдыхаемого воздуха для определения в нем водорода и метана. После этого человеку дают выпить сахаросодержащий субстрат и далее в течение 3 ч каждые 10-20 мин осуществляют дополнительные заборы выдыхаемого воздуха. Предлагалось несколько критериев, способных при выполнении лактулозного дыхательного теста сигнализировать о наличии ИПБТК, однако оказалось, что раннее (до 90-й минуты) повышение концентрации водорода или метана в выдыхаемом воздухе после принятой лактулозы не отличается надежностью. К сожалению, рассматриваемый критерий не позволяет провести различие между ИПБТК и быстрым транзитом. Нормализация показателей дыхательного теста после лечения антибиотиками четко указывают на ИПБТК. Чувствительность и специфичность дыхательного теста варьирует от 17 до 90% и от 44 до 100% соответственно.
Когда для проведения водородного теста в качестве субстрата используют глюкозу, рост концентрации газа более чем на 20 млн-1 обычно рассматривается как признак ИПБТК. Данная проба выявляет только ИПБТК в проксимальном отделе тонкой кишки, так как глюкоза быстро и полностью всасывается уже на этом уровне. Глюкоза до дистальных отделов не доходит, если только нет быстрого пассажа или укорочения тонкой кишки. Таким образом, дыхательный тест с глюкозой может дать ложноотрицательный результат, если ИПБТК ограничено только дистальными отделами тонкой кишки. Ответ на вопрос, приемлем ли тест для клинического разделения между проксимальным и дистальным распространением ИПБТК, пока не получен и требует дальнейшего изучения. Согласно литературным данным, чувствительность и специфичность теста составляют от 27 до 93% и от 36 до 86% соответственно.
Пробная терапия
Если в диагностическом арсенале нет «золотого стандарта», на дополнительную диагностическую информацию можно рассчитывать назначением пробного лечения антибиотиком, особенно у больных с типичной симптоматикой и наличием предрасполагающего к ИПБТК состояния. Исчезновение симптомов после проведенной терапии дает основание думать именно об ИПБТК. Конечно, точно так же можно поступить и в отношении больного при отсутствии явной склонности к ИПБТК, однако интерпретация ответа на лечебные мероприятия и дальнейший план ведения больного в этом случае осложняются. В качестве дополнения к результатам дыхательного теста, свидетельствующим о патологии, у больных с атипичной симптоматикой, когда нет предрасполагающих факторов, можно также прибегнуть к какому-либо другому варианту пробной терапии. Улучшение самочувствия и одновременное возвращение к норме результатов дыхательного теста также доказывает ИПБТК.
Другие тесты
Другие лабораторные критерии ИПБТК неспецифичны. Так, например, в типичном случае выявляют макроцитарную анемию с низкой концентрацией витамина В]2. Содержание фолата и витамина К повышается, так как их синтезируют микробы. Может отмечаться стеаторея, которую подтверждают количественным определением жира в кале или микроскопией свежего стула с окраской на жир. Если в качестве причины ИПБТК предполагается патология, изменяющая анатомию, прибегают к соответствующим визуализирующим исследованиям, в том числе изучают пассаж бария по кишечнику, проводят энте-роклиз и/или КТ/МРТ-энтерографию. При ИПБТК эндоскопические данные и биопсия с гистологией тонкой кишки обычно нормальны, но в этих исследованиях может быть смысл, когда нужно исключить целиакию и болезнь Крона. И то и другое может выступать в качестве причины синдрома мальабсорбции. Анализ кала позволяет исключить инфекционную природу болезни, в то время как определение моторной функции/времени транзита призвано выявлять нарушения моторики ЖКТ.
Дифференциальная диагностика
Тот факт, что многие болезни, предрасполагающие к ИПБТК, сопровождаются симптомами, которые ничем не отличаются от проявлений ИПБТК, чрезвычайно расширяет круг дифференциальной диагностики. Например, парез желудка, хронический панкреатит, ВЗК, целиакия, хроническая мезентериальная ишемия способствуют ИПБТК и в то же самое время дают о себе знать такой же клинической картиной, что и ИПБТК, даже когда ИПБТК нет.
Лечение
Лечение ИПБТК различается в зависимости от характера патологии, на фоне которой она развивается. Лечение подразумевает питательную поддержку, антибактериальную терапию и профилактику рецидива ИПБТК. Главная цель состоит в том, чтобы, насколько это возможно, устранить лежащую в основе патологию тонкой кишки. В редких случаях, когда имеют место анатомические изменения или развиваются осложнения после хирургического вмешательства, этого можно достичь хирургическим путем. Коррекция нарушенной моторики также входит в число сложных проблем, так как эффективных прокинетиков с хорошей переносимостью мало. Для лечения ИПБТК, связанной со склеродермией, описывают успешное применение низких доз октреотида в форме подкожных инъекций.
Когда ИПБТК приводит к дефицитным состояниям, к антибактериальному лечению дополнительно подключают специальные питательные смеси. К обычным мерам относятся исключение лактозы и уменьшение количества неперевариваемых углеводов. Считается, что рацион с высоким содержанием жира, малым количеством углеводов и волокон способен обеспечить достаточный калораж людям, нуждающимся в дополнительном питании, и такой рацион предоставляет меньше ферментируемых субстратов для микроорганизмов, хотя прямых публикаций по этой тематике нет. Если формируется дефицит микронутриентов, в рацион рекомендуют вводить соответствующую добавку.
Антибиотикотерапия - камень преткновения в ведении больного, страдающего ИПБТК. Она рассчитана на уменьшение микробной нагрузки и на симптоматическое улучшение. Выбор антибиотика должен ориентироваться на широкий спектр микрофлоры при ИПБТК. Препарат должен действовать как на аэробные, так и на анаэробные кишечные бактерии. Особой необходимости в определении чувствительности к антибиотикам бактерий из тонкой кишки нет, так как микробы в аспирате при ИПБТК всегда многочисленны и их штаммы обладают различной чувствительностью. В связи с этим рекомендуется сразу назначить эмпирическое лечение в виде 7-10-дневного курса одним из антибиотиков. Если терапия назначена удачно, применение антибиотика обычно купирует симптоматику, часто на долгий срок (на несколько месяцев). Тем не менее определенная доля больных, прежде чем появятся признаки ответа на терапию, требует более длительного приема антибиотика, иногда в зависимости от предрасполагающих состояний необходим курс терапии на несколько месяцев (например, больной принимает препарат 7-10 дней каждого месяца). В таких случаях, чтобы предотвратить развитие резистентности, рекомендуют придерживаться принципа ротации трех или четырех различных антибиотиков, хотя рандомизированных контролируемых испытаний, которые поддержали бы эту общепринятую тактику, практически нет.
Ключевые аспекты ведения больного
- ИПБТК - состояние, которое все чаще распознают в качестве причины синдрома мальабсорбции, но, по всей видимости, недооценивают как фактор в патогенезе широкого круга неспецифических желудочно-кишечных расстройств.
- Распространенность ИПБТК и ее связь с тяжелыми клиническими состояниями до конца не выяснена. Причина, кроме прочего, - в разночтениях как относительно диагностики, так и трактовки самого понятия. Наряду с этим имеет место и значительное наложение клинических проявлений ИПБТК на симптоматику многих других болезней ЖКТ.
- Самые важные факторы в патогенезе ИПБТК - нарушение моторики кишечника и патология ЖКТ, изменяющая анатомию органов. Все это предрасполагает к задержке содержимого кишечника. Имеет также значение недостаточное кислотообразование.
- Классическая симптоматика ИПБТК в виде мальабсорбции в настоящее время встречается редко. Большинство больных предъявляет неспецифические жалобы. Их беспокоят боли в животе или дискомфорт, обильное отхождение газов и вздутие живота, изменение стула при отсутствии явной патологии. Наиболее приемлемый диагностический подход при ИПБТК не выработан. Все пока лишь обсуждается, притом что ни вполне надежных тестов, ни истинного «золотого стандарта» на сегодняшний день нет.
- В лечении ИПБТК крайне важны учет предрасполагающих состояний, обеспечение максимально адекватного поступления питательных веществ в организм, антибиотикотерапия и профилактика рецидивов ИПБТК.
Основной составляющей всей микрофлоры тонкого кишечника является аэробная микрофлора, которая попадает сюда нисходящим путем из ротоглотки, пищевода, желудка. Количество микроорганизмов в 1 мл кишечного сока приблизительно насчитывает 103-105 бактерий в норме. В норме бактериальный состав тонкого кишечника представлен бифидобактериями, дрожжеподобными грибами, бактероидами.
Самая ответственная роль в нормальном функционировании тонкого кишечника, конечно, принадлежит бифидобактериям. Они не только защищают стенки кишечника от других опасных микроорганизмов и помогают в пристеночном пищеварении, но также вырабатывают жизненно необходимые для человека витамин группы В, фактор Касла (К), отвечающий за свертываемость крови. Также эти бактерии помогают усваивать витамин Д, такие микроэлементы как кальций и железо.
Еще бифидобактерии помогают связывать и выводить из организма ядовитые вещества (скатол, индол), появляющиеся в результате нарушения пищеварения, процесса брожения и разложения пищи. Предупреждают развитие аллергии, нарушая трансформацию гистидина в гистамин, который способен запускать развитие аллергии в организме. А также способствуют производству интерферона, повышают активность иммунных клеток.
При возникновении неблагоприятных факторов нормальная микрофлора может чрезмерно размножаться, а впоследствии, и вовсе замещается бактериями не свойственными тонкому кишечнику, а более привычными для толстого отдела кишечника. Тонкий кишечник может становиться таким же густозаселенным бактериями, как и толстый, что приводит к срыву всех функции, возложенных на этот участок желудочно-кишечного тракта.
Факторы, способствующие возникновению СИБР
Данный процесс не может возникнуть на фоне отличного общего состояния организма, и наблюдается только у пациентов с нарушениями либо в самом пищеварительном тракте, либо в других физиологических системах. Чаще всего этому явлению способствуют:

Не стоит умалять и роль правильного питания, отсутствия вредных привычек, активного образа жизни и других основ поддержания хорошего состояния здоровья. Ведь здоровый организм имеет все шансы компенсировать, даже некоторые серьёзные патологии, за счет резервных сил.
Основные этапы развития СИБР
С первыми изменениями в количественном и качественном составе микрофлоры тонкого кишечника нарушаются все процессы и функции этого отдела пищеварительной системы, так:
- Нарушается пищеварение, в результате поглощением бактериями витаминов и полезных веществ у пациентов возникает полиавитаминоз;
- Микрофлора тонкого кишечника продуктами своей жизнедеятельности нарушает активность желчи, что приводит к несостоятельности переваривания жиров и нарушению пищеварения в целом, частым явлениям диареи;
- Плохо переваренная пища не может правильно утилизироваться, это приводит к гниению, брожению в ходе которых появляется большое количество кишечных ядов – это приводит к общей интоксикации организма;
- Чрезмерная секреция расплодившимися микроорганизмами фактора Касла, вызывает повышенную свёртываемость крови, что крайне опасно для беременных женщин, людей склонных к заболеваниям сердечно-сосудистой системы;
- Бактерии способны поглощать из пищи белок, что приводит к белковому голоданию пациента, нарушает общий обмен веществ, приводит к снижению масс тела;
- Нарушения всасывания железа может привести к железодефицитной анемии, а недостаток усваивания кальция и нарушения синтеза витамина Д приводит к хрупкости и изменению костной структуры.
Все эти процессы развиваются в плотной зависимости друг от друга, способствуют нарастанию патологических процессов. Нарушение пищеварения в тонкой кишке, влечет за собой те же проблемы в толстом кишечнике, так что патогенез практически бесконечный. Нарушается вся цепочка процессов в пищеварительном тракте.
Классификация СИБР

Синдром избыточного бактериального роста классифицируют по степени тяжести патологического состояния. Выделяют три степени:
- Легкая. Наблюдается увеличение числа микроорганизмов, которые являются привычными обитателями тонкого кишечника;
- Средняя. Количество аэробных бактерий повышено, также есть анаэробные микроорганизмы;
- Тяжелая. Основное количество микроорганизмов анаэробы. Состав микрофлоры тонкого кишечника становится близким к составу толстого.
Когда можно заподозрить СИБР у пациента
Все симптомы данного патологического состояния можно разделить на две большие группы – абдоминальные (проявляются со стороны органов брюшной полости) и общие (могут иметь отношение к любой системе органов, и организму в целом).
К абдоминальным симптомам относят:
- Возникающее практически сразу после приема пищи вздутие, урчание в животе;
- Часто возникающие диареи;
- Наличие в кале непереваренных частей пищи;
- «Маслянистый» кал, все каловые массы покрыты пленкой жира;
- Редко наблюдается тошнота.
К общим симптомам можно отнести:
- Беспричинное снижение массы тела;
- Авитаминоз, железодефицитную анемию;
- Ухудшение сумеречного зрения;
- Повышение свёртываемости крови;
- Упадок сил, боли в голове, плохое самочувствие;
- Остеомаляция и остеопороз в результате недостатка витамина Д;
- Частые и обширные отеки в результате кишечной потери белков.
Также иногда СИБР может наблюдаться у пациентов с гломерулонефритом, артритом, стеатозом печени и даже гепатита.
Диагностика СИБР

Первое, что постарается установить врач у пришедшего на прием пациента – жалобы, анамнез жизни и заболевания. Здесь, помимо проявлений заболевания и присутствующих жалоб у больного, большое значение играет, проводилось ли ранее хирургическое вмешательство на кишечнике, какие хронические болезни есть у пациента. Когда возникли первые нарушения в работе пищеварительного тракта. Также врач может поинтересоваться, есть ли у пациента вредные привычки, и какой образ жизни он ведёт.
После опроса врач назначит необходимые анализы. Чаще всего перечень обязательных исследований при подозрении на СИБР выглядит так:
- Общий анализ крови. Здесь подтвердить СИБР может макроцитарная либо микроцетарная анемия;
- Биохимический анализ крови. Особое внимание здесь стоит обратить на содержание витамина В12 и фолиевой кислоты. Если показатели В12 снижены, а фолиевой кислоты в избытке можно заподозрить СИБР;
- Анализ мочи. Если наблюдается повышение количества 4-гидроксифенилацетоновой кислоты – это плохой признак;
- Дыхательные тесты с ксилозой, желчной кислотой и водородной. Повышение количества водорода в выдыхаемом воздухе при данных пробах может свидетельствовать о чрезмерной обсеменённости тонкого кишечника микрофлорой;
- Копрологические исследования. При данной патологии, может наблюдаться смещение РН каловых масс в кислую сторону;
- Исследования кала на стеаторею позволяет выявить повышенное число жира в каловых массах;
- Специальный тест с Д-ксилозой. Пациент принимает внутрь Д-ксилозу, через час берут венозную кровь, а в течение 5 часов собирают мочу. Оценивают количество выведенной Д-ксилозы;
- Тест Шиллинга. Больному дают внутрь В12, после чего оценивают скорость выведения и количество усвоенного.
Также врач может назначить проведение инвазивных методов исследования тонкого кишечника. Чаще всего это биопсия, которая позволяет выявить атрофию ворсинок кишечника и гиперплазию крипт, а также скопление лимфоцитов в слизистой кишечника.
Самым информативным методом является посев содержимого тонкой кишки, полученного путем аспирации. Если показатель числа бактерии в посеве выше 10 5 клеток/мл, это объективное доказательство, подтверждающее наличие СИБР.
Лечение СИБР, коррекция микрофлоры тонкого кишечника

Для эффективности терапии патологии следует применять комплексный подход к лечению. Успеха можно достичь, объединив антибиотикотерапию, коррекцию питания, а также методы повышения перистальтики.
Антибиотикотерапия. Чаще всего курс лечения составляет 14 дней, однако при снова появляющихся симптомах возможно повторение терапии. Выбирая антибиотики, следует отдавать предпочтение препаратам, имеющим воздействие, как на аэробную, так и на анаэробную флору.
Наиболее часто, применяют антибиотики тетрациклинового ряда, цефалексин, рифаксимин, амоксицилин клавулоновую кислоту, метронидазол, триметоприм и другие. При неэффективности одного препарата, по решению врача, может применяться другие лекарственные средства.
Также к антибиотикам эффективно подключить адсорбенты, которые помогут в выведении балластных веществ на 10-14 дней. По завершению курса приема лекарственных препаратов, стоит пройти лечение эубиотиками и пробиотиками для заселения нормальной микрофлоры в тонкий кишечник, и создания подходящих условий для их размножения.
Коррекция питания. Желательно включать в свой рацион продукты, прошедшие минимальную термообработку. В рацион отлично впишутся все сорта рыб, мясо, птица, яйца. Желание полакомиться произведениями кондитерского искусства можно утолить фруктами и ягодами.
Можно включать в свой рацион свежие овощи. Молочные продукты следует не употреблять или включать в минимальных количествах. Также необходимо ограничить себя в продуктах, богатых рафинированным сахаром, транс жирами и другими вредными компонентами.
Благотворно также будет дробное питание небольшими порциями с минимальными промежутками. Не лишним будет взять в привычку кушать каждый день в одно и то же время, так организм сможет максимально подготовиться к качественному перевариванию пищи.
Также стоит употреблять продукты богатые витаминами, либо принимать препараты, содержащие их, для компенсации авитаминоза, вызванного значительным количеством микроорганизмов.
Вредное влияние оказывает также частое переедание, желудочно-кишечный тракт просто не способен справиться с огромным количеством пищи, что может вызвать нарушение пищеварения и привести к гибели хорошей микрофлоры, как следствие нарушение биоценоза.

Улучшение перистальтики. Любая физическая активность способствует усилению сокращений кишечной стенки. Не важно, будь-то пешая ходьба, или фитнес - всё будет оказывать благотворный эффект на работу органов пищеварения.
Особенно полезными окажутся упражнения на укрепление мышц спины и брюшного пресса, а также на улучшение тонуса мышц малого таза. Вращение хула-хупа, скручивания, планки – не только помогут кишечнику, но и сделают более здоровым весь организм, повысят иммунитет, а значит, дадут возможность организму компенсировать все проблемы.
Однако стоит понимать, что все эти мероприятия будут оказывать лишь временный результат, и не исправят ситуацию в целом, до тех пор, пока не будут устранены причины СИБРа. Так, если наблюдается изменение анатомии кишечника, то пока хирург не проведет оперативное вмешательство и не исправит дефект, ни лекарственные препараты, ни питание не окажут должного эффекта.
Если к чрезмерному размножению бактерий привела пониженная кислотность желудка или недостаточное количество соляной кислоты, то в первую очередь нужно устранить эти вопросы, и только потом вплотную браться за нормализацию микрофлоры кишечника.
Увеличение роста патогенных микроорганизмов и условно патогенных это всегда системная проблема. Если эти нарушения развились на фоне снижения иммунитета, то необходима иммунокоррекция и мероприятия, направленные на общее оздоровление организма.
Закаливание, избегание стрессовых ситуаций, частое пребывание на свежем воздухе, физически активная, насыщенная жизнь поможет сохранить здоровье кишечника и всего организма надолго.
Следите за своим здоровьем, вырабатывайте полезные привычки и при первых же признаках того, что в организме что-то не ладно, не стесняйтесь обратиться к врачу за специализированной помощью. Будьте здоровы!
Синдром избыточного роста бактерий (СИБР) в тонком кишечнике - патология, обусловленная повышенным заселением тонкой кишки преимущественно фекальными бактериями, и приводящая к множественным расстройствам пищеварения. Данное заболевание является, как правило, последствием других нарушений жизнедеятельности организма, повлекших его за собой.
Общие сведения о заболевании СИБР
В здоровом состоянии тонкий кишечник имеет довольно малую плотность заселения бактериями, допустимой нормой считается не более 10 5 бактерий на 1 мл аспирированного содержимого тонкой кишки. При этом основная часть микрофлоры тонкого кишечника состоит из грамположительных аэробных микроорганизмов. Оптимальный уровень содержания бактерий обеспечивается функцией илеоцекального клапана, выделением слизи и соляной кислоты и нормальной активностью перистальтики. При возникновении синдрома изменяется не только количественная, но и качественная составляющая микрофлоры, наблюдается существенное преобладание грамотрицательных микроорганизмов. Заболевание корректируется с помощью антибактериальных препаратов.
Степени заболевания
Выделяют следующие степени тяжести заболевания:
- увеличение кишечной микрофлоры с преобладанием аэробных микроорганизмов, нуждающихся в воздухе для осуществления своих жизненных процессов;
- при наличии повышенного аэробного микробиоценоза кишечника возникают анаэробные микробы, не имеющие необходимости в воздухе;
- повышенный микробиоценоз кишечника с подавляющим большинством анаэробных бактерий.
Причины возникновения болезни
 Чрезмерное упоребление антибиотиков может спровоцировать СИБР.
Чрезмерное упоребление антибиотиков может спровоцировать СИБР. Причинами возникновения синдрома бывают:
- стрессовые обстоятельства (изменение места жительства, неблагоприятная экология, длительные стрессы и нервные расстройства);
- заболевания, снижающие иммунитет (алкоголизм, наркомания, СПИД);
- гиповитаминоз;
- излишнее употребление антибиотиков;
- расстройства функционирования илеоцекального клапана (функциональная недостаточность, воспаления и опухоли);
- очищения организма с помощью обширных клизм (например, гидроколонотерапия), популярные в качестве средства для снижения веса;
- расстройства моторики ЖКТ (нарушения проходимости, стаз содержимого кишечника);
- последствия хирургического вмешательства (ваготомия, резекция, холецистэктомия, слепые петли кишечника, кишечные свищи и прочие обструкции).
Основные симптомы СИБР
Распространенными симптомами синдрома чрезмерного бактериального заселения кишечника считаются:
- со стороны ЖКТ - тошнота, вздутие живота, метеоризм, диарея, боль в нижней части живота;
- снижение массы тела вследствие мальабсорбции (нарушения всасывания) жиров;
- отечность, обусловленная белковой недостаточностью;
- гиповитаминоз, особенно жирорастворимых витаминов А, D, Е, К и витамина B12, активно потребляемого бактериальной флорой;
- со стороны нервной системы - слабость, плохой сон, утомляемость, головная боль.
Перечисленные симптомы не всегда проявляются в полной мере и у некоторых пациентов заболевание протекает без ярко выраженной симптоматики. Однако снижение веса и гиповитаминоз присутствуют практически всегда, поскольку расстройство усвоения жиров при СИБР неизбежно.
Прогноз СИБР и возможные осложнения
Прогноз синдрома немаловажен и в основном формируется в зависимости от течения болезни - первопричины, вызвавшей его. В запущенном виде синдром избыточного бактериального роста способен привести к серьезным осложнениям. Следует помнить, что даже в случае успешной терапии вероятность рецидива избыточного бактериального роста довольно высока, особенно если первопричина заболевания не устранена полностью. Поэтому важно придерживаться профилактических мер.
Осложнения СИБР - синдром недостаточности пищеварения и синдром недостаточности питания, что приводит к снижению массы тела, гиповитаминозу и общему истощению организма. Длительный недостаток витамина B12 способен привести к снижению уровня гемоглобина и эритроцитов в крови и развитию макроцитарной анемии.
Диагностика синдрома избыточного бактериального роста в кишечнике
Методы лабораторной диагностики
Для точного диагноза необходимо сдать анализы крови, мочи и кала.
Лабораторная диагностика включает проведение следующих исследований:
- анализы крови - обобщенный (для обнаружения признаков наличия воспалительных процессов) и биохимический (показателен при наличии первичной патологии, спровоцировавшей появление избыточного бактериального роста);
- анализ мочи (диаграмма химического состава урины также может указать на рост объема );
- анализ кала (проверяется преимущественно на содержание жира, что показательно поскольку недуг является причиной мальабсорбции жиров).
Методы инструментального исследования
С целью выявления патологии кишечника могут быть применены следующие методы инструментального исследования:
- ирригоскопия (рентгенологическое исследование проходимости кишечника с помощью контрастного вещества);
- сонография (ультразвуковое исследование кишечника на наличие повреждений);
- тест Шиллинга (оценка абсорбции витамина B12 путем введения его пациенту и оценивания выводимого с мочой объема неусвоенного витамина);
- биопсия тощей кишки (анализ образца ткани кишечника на симптомы патологических изменений слизистой оболочки, вызванных ростом микрофлоры);
- эндоскопия (получение аспирата и исследование содержимого тощей кишки на посев бактерий) - метод дает наиболее точное представление о концентрации микроорганизмов на исследуемой территории.
На практике чаще используются дыхательные тесты, ввиду их большей доступности.
Микроорганизмы продуцируют большое количество газов, что позволяет успешно использовать дыхательные тесты для выявления синдрома чрезмерного роста микрофлоры в ЖКТ путем измерения концентрации газов в выдыхаемом пациентом воздухе. Дыхательные тесты экспрессивны, не требуют специализированного оборудования и значительных финансовых затрат. Проведение таких тестов предполагает соблюдение определенных правил: отказ от употребления пищи, богатой углеводами, минимум за 12 ч до исследования, воздержание от физических нагрузок и табакокурения минимум за 3 ч до теста и запрет на использование антибактериальных средств для полости рта.
Перед прохождением дыхательных тестов необходимо исключить из рациона углеводы и физические нагрузки.
Для дыхательных проб используются следующие вещества:
- Холеглицерин, меченый углерод или ксилоза. При использовании какого-либо из указанных веществ измеряется углекислый газ в выдыхаемом воздухе, чувствительность теста составляет около 70%.
- Глюкоза или лактулоза. В этом случае измеряется содержание водорода и тесты с использованием этих веществ более надежны. Однако глюкоза менее показательна, поскольку не достигает дистальных отделов тощей кишки, полностью усваиваясь в проксимальных отделах. Лактулоза без абсорбции достигает толстой кишки и дает более полную картину. Чувствительность и специфичность теста с лактулозой достигает 86 и 91% соответственно, что является наиболее высоким показателем среди дыхательных проб.
Желудочно-кишечный тракт организма засеян несколькими сотнями различного вида бактерий. Состав микроорганизмов разнится в отделах более или менее удаленных от медианной плоскости тонкого кишечника. Микрофлора имеет большое значение для нормализации бесперебойной работы кишечника. Для человека без отклонений в состоянии здоровья, как правило, различные микроорганизмы служат для поддержания в нормальном состоянии кислотно-щелочного равновесия в желудке, способствуют выработке желудочного сока для переработки пищи, контролируют двигательную активность тонкой кишки. В случае сбоя в работе хоть одного из этих устройств, возникает высокая вероятность формирования синдрома избыточного бактериального роста в тонкой кишке.
Определение
Чрезмерный бактериальный рост в тонком кишечнике возникает как следствие изменений, связанных с анатомией человека, или при нарушениях двигательной активности кишечно-желудочного тракта и недостаточности желудочной секреции. Возникшие нарушения могут привести к проблемам с питанием, убытку витаминов и к сбоям переваривания жиров. Лечится синдром бактериальной избыточности применением антибактериальных препаратов.
Симптоматика
 Вздутие живота – одним из симптомов заболевания.
Вздутие живота – одним из симптомов заболевания. Больные с избыточным синдромом роста бактерий наблюдают следующие симптомы:
- болезненное вздутие живота, урчание, которые возникают спустя небольшое время после употребления пищи;
- преимущественно понос;
- плохо переваренная пища в каловых массах;
- наличие в каловых массах вкраплений жира;
- снижение зрения;
- в редких случаях наблюдается тошнота;
- упадок сил;
- головные боли;
- резкое похудение;
- ощущение беспокойства, паника;
- преимущественно плохое настроение;
- головокружение;
- депрессивное состояние.
Формы заболевания
Бактериальное повышение в тонких кишках зависит от количества и характера микрофлоры и бывает трех степеней:
- Первая степень является аэробной, т. е., для выполнения жизненных функций группы живых организмов, невидимых невооруженным глазом, необходим кислород, с увеличенной микрофлорой кишечника.
- Вторая степень в синдроме представляет собой аэробную кишечную увеличенную микрофлору с образованием бактерий. В данном случае кислород для выполнения жизненных функций микроорганизмов не потребуется.
- Третья степень имеет большинство анаэробной микрофлоры.
Источник возникновения заболевания
Тонкая кишка с синдромом избыточного бактериального роста -явление, которое может возникнуть по ряду причин. В основном причины подразделяют на те, которые изучают происхождение заболевания, их условия, а также те, которые основаны на изучении развития болезни.
 Возможная причина бактериального роста.
Возможная причина бактериального роста. По этиологии выделяют следующие причины бактериального роста:
- избыточный уровень бактерий в кишке может возникнуть после проведенных операций;
- нарушения в функциональности Баугиниевой заслонки;
- болезни пищеварительной системы, которые связанны с двигательной активностью кишечника;
- продолжительное пищевое нарушение;
- повреждения в полости кишечника под воздействием ферментов пищеварения и всасывания;
- структура кишечника, а именно сужение его просвета;
- различные пищевые непереносимости;
- воспалительные заболевания хронической формы в кишечнике;
- обструкции;
- симптомокомплекс хронических расстройств;
- дивертикулярная болезнь;
- цирроз печени;
- алкоголизм;
- вагатомия;
- продолжительное употребление медикаментов, снижающих иммунную систему человека;
- избыточная терапия антибиотиками;
- бактерии, которые поступают из внекишечного вместилища;
- всевозможные стрессы;
- нарушения иммунной системы местного и системного характера;
- сахарный диабет.
В результате воздействия этиологических признаков, происходит нарушение защитительного слоя слизистой оболочки тонкой кишки. Вследствие этого вызываются локальные и системные процессы патологии, нарушается защитное назначение слизистой оболочки и функционирование пищеварительных ферментов. Помимо этого, происходит расстройство секреции, окисление жирных кислот, эндогенная интоксикация.
При серьезных нарушениях иммунной системы человека может произойти обмен бактерий в лимфу и кровь, с последующим развитием воспаления с гноем на всевозможных тканях и органах.
Проведение диагностирования и лечение
Диагностирование позволяет поставить точный диагноз и констатировать о чрезмерном бактериальном росте. Таким образом, диагностика может включать в себя:
- Сбор информации о семье больного, чтобы выявить по родственной связи наличие болезней, связанных с пищеварительной системой.
- Анализирование жалоб пациента и прошлых болезней, а также изучение стула больного (консистенция, длительность). Помимо этого, учитывается метеоризм, тошнота.
- Визуальный осмотр пациента, который основан на оценке цвета кожи больного, телосложения и определение наличия лишнего веса.
- Сбор информации об имеющихся заболеваниях кишечно-желудочного тракта и перенесенных операциях и других заболеваниях.
 Тест Шиллинга выявляет B12-дефицитную анемию.
Тест Шиллинга выявляет B12-дефицитную анемию. Диагностирование в обязательном порядке включает в себя лабораторные исследования, которые основаны на сдаче крови на общий анализ, который покажет или опровергнет малокровие, повышение уровня лейкоцитов, что бывает при воспалительном процессе в организме. Помимо этого, следует провести биохимический анализ крови, который позволит выявить первопричину заболевания, общий анализ мочи, что необходимо для определения повышения возможных химических веществ, указывающих на развитие превышающих норму бактерий. Для постановки точного диагноза и определения первопричины важно провести анализ канала, который укажет на наличие или отсутствие непереваренной пищи, определит кислотность кала и количество в нем жира.
Важным исследовательским методом является дыхательный тест. Перед проведением которого следует придерживаться ряда правил: запрещается употреблять пищу с наличием углеводов вечером перед тестированием; не курить и не перегружать организм физическими нагрузками за несколько часов до теста; ополаскивать полость рта с антибактериальным действием прежде чем приступать к тестированию. Еще одним не менее важным методом диагностирования является тест с сахаром, который покажет в бактериальном росте водород, а также тест с ксилозой, который необходим для обнаружения меченого углекислого газа.
Диагностирование синдрома избыточного бактериального роста основано на инструментально исследовании:
- Рентген, который необходим для выявления дивертикулеза или сужения тонкой кишки.
- Тест Шиллинга, который заключается в приеме пациентом витамина В12 и после чего он выводится с мочой. Врач оценивает всасывание витамина.
- Биопсия тонкой кишки. Для этого берется кусочек ткани и направляется на исследование под микроскопом. Если диагноз заболевания подтверждается, происходит ненормальное изменение слизистой кишечника.
При чрезмерном росте бактерий необходима консультация следующих специалистов:
- хирург, который исключит хирургические патологии;
- гинеколог – необходим, чтобы исключить патологии гинекологического характера;
- уролог, консультация с которым исключит мочевыделительные патологии;
- инфекционист, консультация с которым проводится при наличии показаний и необходима для исключения диареи инфекционного характера.
 Немедикаментозное лечение заключается в соблюдении необходимой диеты.
Немедикаментозное лечение заключается в соблюдении необходимой диеты. Лечение повышенного бактериального роста в тонкой кишке основано на уменьшении или полной ликвидации симптоматики первичного заболевания, на устранении чрезмерного наличия бактерий в тонкой кишке, восстановлении микробиоценоза и нормализации функционирования пищеварительной системы. Терапия может осуществляться с помощью медикаментов и без нее.
Немедикаментозное лечение заключается в соблюдении необходимой диеты и употреблении продуктов питания естественного происхождения. К таким продуктам относится кисломолочная продукция с бифидобактериями. Лечение синдрома лекарственными препаратами основано на терапии антибактериальными препаратами, пробиотиками, пребиотиками. При необходимости назначается внутривенное введение витаминотерапии.
Хирургическое вмешательство проводится в случае безрезультатного медикаментозного и немедикаментозного лечения.
Для цитирования:
Белоусова Е.А. Синдром избыточного бактериального роста тонкой кишки при хроническом панкреатите // РМЖ. 2009. №5. С. 317
Введение Хронический панкреатит (ХП) рассматривается как заболевание с комплексом тяжелых симптомов, среди которых доминируют боль и экскреторная недостаточность поджелудочной железы (ЭНПЖ). Причинами развития этих синдромов является хроническая обструкция панкреатических протоков разной степени выраженности, затрудняющая поступление панкреатического сока в двенадцатиперстную кишку. Не-из-бежно ЭНПЖ сопровождается нарушением переваривания и всасывания нутриентов, что может привести к развитию мальабсорбции. Считается, что адекватная терапия ферментными препаратами должна компенсировать дефицит эндогенных ферментов и восстановить нормальное пищеварение. Однако на практике далеко не всегда удается легко справиться с ЭНПЖ. Основная причина этого, как правило, связана с недостаточной дозой ферментных средств или выбором малоэффективного препарата. Существует и вторая, очень серьезная причина упорного течения ЭНПЖ и низкой, на первый взгляд, эффективности ферментной терапии. Это связано с развитием синдрома избыточного бактериального роста в тонкой кишке (СИБР), известного в англоязычной литературе как «bacterial overgrowth». СИБР мало известен широкому кругу врачей и не учитывается в лечебной тактике. Поэтому целью данной статьи было ознакомить терапевтов и гастроэнтерологов с современными подходами к коррекции СИБР при ХП.
Хронический панкреатит (ХП) рассматривается как заболевание с комплексом тяжелых симптомов, среди которых доминируют боль и экскреторная недостаточность поджелудочной железы (ЭНПЖ). Причинами развития этих синдромов является хроническая обструкция панкреатических протоков разной степени выраженности, затрудняющая поступление панкреатического сока в двенадцатиперстную кишку. Не-из-бежно ЭНПЖ сопровождается нарушением переваривания и всасывания нутриентов, что может привести к развитию мальабсорбции. Считается, что адекватная терапия ферментными препаратами должна компенсировать дефицит эндогенных ферментов и восстановить нормальное пищеварение. Однако на практике далеко не всегда удается легко справиться с ЭНПЖ. Основная причина этого, как правило, связана с недостаточной дозой ферментных средств или выбором малоэффективного препарата. Существует и вторая, очень серьезная причина упорного течения ЭНПЖ и низкой, на первый взгляд, эффективности ферментной терапии. Это связано с развитием синдрома избыточного бактериального роста в тонкой кишке (СИБР), известного в англоязычной литературе как «bacterial overgrowth». СИБР мало известен широкому кругу врачей и не учитывается в лечебной тактике. Поэтому целью данной статьи было ознакомить терапевтов и гастроэнтерологов с современными подходами к коррекции СИБР при ХП.
Нормальная микрофлора
желудочно-кишечного тракта
С современных позиций нормальную микрофлору человека (нормофлора, микробиота) рассматривают как совокупность множества микробиоценозов, занимающих многочисленные экологические ниши (биотопы) на коже и слизистых оболочках всех полостей организма, открытых внешней среде . Общая численность бактерий у взрослого человека составляет 1015 клеток, что более чем в 10 раз превышает количество собственных клеток макроорганизма. Суще-ствую-щий в настоящее время нормативный документ «Рос-сий-ский отраслевой стандарт по дисбактериозу» предлагает следующее определение нормофлоры: это «ка-чественное и количественное соотношение разнообразных популяций ми-кробов отдельных органов и систем, поддерживающих биохимическое, метаболическое и иммунологическое равновесие макроорганизма, необходимое для сохранения здоровья человека» . Из этого определения следует, что нормофлора каждого биотопа выполняет многочисленные функции не только по поддержанию его функционирования, но и гомеостаза организма в целом.
Видовой и количественный состав микрофлоры каждого биотопа желудочно-кишечного тракта (ЖКТ) достаточно постоянен вследствие влияния многочисленных защитных факторов как со стороны организма хозяина, так и собственно микробиоты :
. Генетическая предрасположенность
. Кислая желудочная среда
. Нормальная моторно-эвакуаторная функция ЖКТ
. Анатомические сфинктеры ЖКТ
. Постоянный уровень внутрипросветного рН в разных биотопах
. Состояние иммунной системы слизистых оболочек
. Бактерицидные вещества, вырабатываемые слизистыми оболочками (лизоцим, лактоферрин и др.)
. Фагоцитарная активность макрофагов слизистой оболочки
. Секреторный IgA
. Бактериальные колицины и микроцины (эндогенные пептидные антибиотики микробного происхождения)
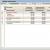
Только в ЖКТ человека обитает более 400 видов бактерий - представителей 17 различных семейств . Пище-ва-рительный тракт человека заселен бактериями неравномерно, состав микрофлоры разных биотопов представлен в таблице 1.
Как видно из таблицы, самая высокая плотность микробного обсеменения в толстой кишке - около 400 различных видов. Общая биомасса микробных клеток толстой кишки составляет приблизительно 1,5 кг, что соответствует 1011-1012 КОЕ/г содержимого и составляет около 1/3 сухого веса фекалий . Именно толстая кишка в силу такой высокой обсемененности несет самую большую функциональную нагрузку по сравнению с другими биотопами. Содержание бактерий в верхних отделах кишечника колеблется в узком интервале 103-104 КОЕ/мл кишечного содержимого. Основ-ную массу бактерий в толстой и нижних отделах тонкой кишки составляют в сумме бактероиды, эубактерии, бифидобактерии, пептострептококки, руминококки, клостридии и лактобактерии, а в верхних отделах тонкой кишки - бактероиды, лактобактерии и кокки (табл. 1).
Несмотря на относительно небольшое количество микроорганизмов в проксимальной тонкой кишке их функции для жизнедеятельности этого биотопа очень важны, в частности, для поддержания просветного pН и иммунного статуса слизистой оболочки. Нормальная микрофлора ЖКТ в целом выполняет метаболические, защитные, антимутагенные и антиканцерогенные функции. Метаболические и антиканцерогенные функции ложатся в основном на флору толстой кишки, а в реализации антитоксических, защитных и иммунных функций, в поддержании колонизационной резистентности и микробного антагонизма по отношению к патогенам и условным патогенам участвует микрофлора всех биотопов. В равной мере это касается верхних отделов тонкой кишки.
Под колонизационной резистентностью понимают совокупность механизмов, обеспечивающих по-стоянство видового и количественного состава микробных популяций в определенном биотопе, препятствующих размножению условно-патогенной и патогенной флоры и ее транслокации в нехарактерные биотопы и во внутреннюю среду организма. Проявлением такой транслокации микрофлоры может служить СИБР в тонкой кишке с повышением микробной обсемененности последней более 104 КОЕ/мл кишечного содержимого .
Синдром избыточного бактериального роста (синдром избыточной
контаминации - bacterial overgrowth)
Как было сказано выше, нормальное содержание бактерий в верхних отделах кишечника колеблется в уз-ком интервале 103-104 КОЕ/мл кишечного содержимого, и эта величина является своего рода константой для тонкой кишки. Видовой состав микробиоты также до-ста-точно постоянен: бактероиды, лактобациллы, кокки.
Суммируя существующие определения, с нашей точки зрения можно дать следующее определение синдрома СИБР: синдром избыточного бактериального роста - это обсеменение проксимальных отделов тонкой кишки свыше 104 м.к. (КОЕ)/мл кишечного содержимого за счет условно-патогенной микрофлоры, поступающей из верхних отделов ЖКТ (или верхних дыхательных путей) или вследствие ретроградной транслокации условно-патогенных представителей микробиоты толстой кишки .
Следует подчеркнуть, что понятие СИБР в международной литературе относится к избыточному росту флоры только в тонкой, но не в толстой кишке.
Выделяют несколько основных механизмов, приводящих к СИБР . Первый механизм обусловлен гипо- или ахлоргидрией любого происхождения. Сни-жение защитного кислотного барьера позволяет микробам из ротовой полости и верхних отделов респираторного тракта колонизировать желудок и далее - тонкую кишку. В основе этого процесса могут лежать разные причины, но наиболее часто этот путь микробного обсеменения тонкой кишки возникает после резекции желудка или гастрэктомии, при длительном приеме ингибиторов желудочной секреции, при аутоиммунном гастрите, при аутоиммунных заболеваниях, таких как пернициозная анемия и склеродермия.
Второй механизм развития СИБР обусловлен нарушением так называемого «клиренса кишечника», т.е. нарушением способности тонкой кишки элиминировать попавшие в нее патогенные или условно-патогенные микроорганизмы. Нарушение клиренса происходит при снижении активности защитных механизмов, поддерживающих постоянство микробиоты тонкой кишки: угнетение двигательной активности, снижение синтеза бактерицидных веществ и секреторного IgA, снижение фагоцитарной функции макрофагов слизистой оболочки тонкой кишки и др.
Третий механизм связан с ретроградной транслокацией микрофлоры из толстой кишки в тонкую вследствие недостаточности илеоцекального клапана при воспалении или мо-торных нарушениях толстой кишки. Почти любое гастро-эн-терологическое заболевание может привести к развитию СИБР (табл. 2).
Методы оценки СИБР
Диагностика СИБР весьма сложна, т.к. методы забора содержимого тонкой кишки слишком трудоемкие. Для этой цели разработан простой и удобный метод по определению концентрации водорода в выдыхаемом воздухе после углеводной нагрузки глюкозой или лактозой (дыхательный водородный тест) . При наличии СИБР уровень водорода в выдыхаемом воздухе высокий за счет образования микробных метаболитов в тонкой кишке. Этим же методом можно мониторировать результаты лечения различными препаратами, подавляющими рост избыточной флоры в тонкой кишке. Метод дешев, прост в исполнении, однако, к сожалению, не имеет широкого распространения в России.
Хронический панкреатит и СИБР
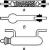
По данным J.E. Dominguez-Munoz, СИБР встречается у 40% больных ХП и является одной из наиболее частых причин, приводящих к недостаточной эффективности ферментной заместительной терапии . Многочисленные механизмы, приводящие при ХП к нарушению переваривания и СИБР, подробно представлены на рисунке 1.
Таким образом, ХП сопровождается:
. нарушением процессов переваривания и всасывания
. развитием избыточного бактериального роста в тонкой кишке
. нарушением моторной функции ЖКТ
Первоначальное нарушение полостного пищеварения при ХП путем взаимодействия сложных механизмов усугубляется нарушением мембранного пищеварения, а все участвующие механизмы действуют по принципу порочного круга.
Лечение синдрома избыточного
бактериального роста
Следует иметь в виду, что СИБР является не самостоятельной патологией, а лишь вторичным синдромом, сопутствующим многим патологическим состояниям. Если при нарушениях микробиоты толстой кишки, как правило, отсутствуют четко выраженные клинические симптомы, то при СИБР обычно имеют место метеоризм, нарушения стула, иногда выраженная диарея. Вместе с тем, все указанные симптомы не специфичны, и связать их однозначно с СИБР не представляется возможным. В контексте данной статьи метеоризм, диарея, стеторея могут в равной мере быть следствием и ЭНПЖ, и СИБР.
В любом случае, микробные нарушения как в толстой, так и в тонкой кишке всегда вторичны, поэтому для их коррекции необходимо прежде всего устранить вы-зы-вающие их негативные факторы (например, лекарственные или экологические влияния) или проводить лечение основного заболевания. Важно подчеркнуть, что коррекция СИБР не является самоцелью и проводится:
. при невозможности устранить его причину
. при действии постоянного агрессивного фактора (например, химиотерапия)
. в качестве дополнительной меры, при недостаточной эффективности лечения основного заболевания, вызвавшего эти нарушения.
Идеальной иллюстрацией этих положений является СИБР, развивающийся на фоне ЭНПЖ. В идеале при назначении адекватной дозы ферментных препаратов восстанавливается переваривание и дополнительная коррекция СИБР не требуется. Однако СИБР является одной из наиболее частых причин, приводящих к недостаточной эффективности ферментной заместительной терапии . В одном из исследований влияние терапии Креоном на СИБР (по данным водородного дыхательного теста) оценивали у 15 пациентов с ЭНПЖ при ХП. Этим больным в течение 2 мес. проводили терапию Креоном 100-150 тыс. МЕ в сутки. У большей части (65% - 10 больных) по данным повторного водородного теста СИБР был ликвидирован, у 53% (8 больных) - исчез метеоризм, у 73% (11 больных) было улучшение самочувствия, но сохранялись диспептические симптомы .
Исходя из вышесказанного назначение адекватных доз эффективных ферментных средств (Креон 25000-40000 МЕ с каждым приемом пищи) должно быть терапией первой линии при заболеванях поджелудочной железы с ЭНПЖ с СИБР или без него. При ее недостаточной эффективности показано назначение препаратов для устранения микробного роста в тонкой кишке.
Лечебная тактика при микробных нарушениях зависит от степени их выраженности, наличия клинических проявлений, транслокации бактерий в другие биотопы. В ряде случаев при наличии СИБР возникает необходимость проведения «селективной микробной деконтаминации кишечника». Это понятие подразумевает проведение санации ки-шеч-ника (деконтаминации) препаратами, селективно подавляющими рост чужеродной флоры и не влияющими на нормофлору. С целью деконтаминации применяют не-сколько групп средств:
. антибактериальные препараты
. непатогенные грибы
. спорообразующие препараты на основе представителей транзиторной флоры
. микробные метаболиты.
Антибиотики
Оптимальный антибактериальный препарат для деконтаминации тонкой кишки и устранения СИБР должен отвечать следующим требованиям:
. иметь минимальную абсорбцию из кишечника
. создавать высокую концентрацию в полости кишки
. обладать селективностью (должен подавлять чужеродную флору и не влиять на нормофлору
. иметь широкий спектр антимикробного действия, включая аэробов и анаэробов
. иметь минимум побочных эффектов и быть безо-пасным
. иметь доказанную клиническую эффективность
Одним их новых в России и наиболее интересным со всех трех точек зрения препаратом является производное рифамицина - препарат рифаксимин (Альфа-нормикс). Это не абсорбируемый (<1%) при приеме внутрь антибиотик, достигающий высоких концентраций в слизистой оболочке ЖКТ. Препарат не действует вне ЖКТ, т.е. является местнодействующим кишечным антисептиком. Рифа-кси-мин хорошо переносится, имеет минимум побочных эф-фек-тов и не вызывает бактериальной резистентности. Препарат имеет широкий спектр антибактериального действия против грамположительных (Enterococcus spp, M. tuberculosis, Streptococcus pyogenes, Streptococcus faecalis, Streptococcus pneumoniae, Staphylococcus epidermidis, Staphylococcus aureus) и грамотрицательных (Escheri-chia coli, Shigella spp, Salmonella spp, Yersinia enterocolica, Proteus spp, Vibrio cholerae) аэробных бактерий и грампо-ло-жительных (Clostridium perfrigens, Clostridium difficile, Peptococcus spp, Peptostreptococcus spp) и грамот-ри-цательных (Bacteroides spp, Bacteroides fragilis, Helico-bacter pylori) анаэробов . Такой спектр действия определяет те-ра-певтические возможности препарата. Таким образом, ри-фак-симин удовлетворяет всем основ-ным требованиям, предъявляемым к идеальному антибактериальному препарату. Он с успехом используется при острых кишечных инфекциях, для санации толстой кишки при «дисбактериозе», для коррекции СИБР, при антибиотико-ассо-ции-ро-ванных поражениях кишечника и при печеночной энцефалопатии. При СИБР, доказанном с помощью водородного дыхательного теста, рифаксимин применяется по 400 мг 3 раза в сутки в течение 7 дней. При этом уровень выдыхаемого водорода снижается в 3-5 раз уже к третьему дню лечения, что свидетельствует о быстрой санации тонкой кишки .
В течение долгого времени для лечения СИБР при разных патологиях использовались разные антибиотики (тетрациклины, линкомицин, ампициллин и др.), которые не обладают селективностью, не действуют на анаэробную флору, быстро всасываются из ЖКТ и имеют широкий спектр побочных эффектов (в том числе антибиотико-ассоциированную диарею) и подавляют нормофлору. Для демонстрации эффективности рифаксимина было проведено двойное слепое исследование, подтверждающее приоритет рифаксимина перед тетрациклином при СИБР . В этом исследовании СИБР в двух группах больных оценивали по водородному дыхательному тесту и определяли пик экскреции водорода в выдыхаемом воздухе и общую концентрацию водорода после нагрузки глюкозой до и через 3 дня после окончания курса антибиотика. Было показано, что при равных начальных уровнях водорода его пик после нагрузки глюкозой, равно как и общая концентрация в выдыхаемом воздухе после лечения, был достоверно ниже у больных, получавших рифаксимин, по сравнению с группой, получавшей хлортетрациклин.
Из других эффективных антибактериальных средств можно назвать производные оксихинолонов, нитрофурановые низкоабсорбируемые призводные (нифуроксазид) и нитроимидазолы (метронидазол, тинидазол) . Хотя последняя группа всасывается из толстой кишки, но, тем не менее, применение ее эффективно, главным образом, при контаминации анаэробными микроорганизмами. Длитель-ность курса деконтаминации при СИБР составляет 12-14 дней.
Непатогенные грибы
При непереносимости антибактериальных препаратов возможно и эффективно назначение средств на основе непатогенных дрожжевых грибков рода S. boulardii. В то же время S. boulardii не подавляют рост облигатных микроорганизмов в полости кишки и устойчивы к действию соляной кислоты. При ежедневном приеме они обнаруживается во всех отделах ЖКТ, в том числе в тонкой кишке. Эти дрожжи являются для человека транзиторной флорой, поэтому через 2-5 дней после окончания приема препарата полностью выводятся из организма без побочных явлений. Препарат не всасывается из просвета ЖКТ и является местнодействующим кишечным антисептиком. Анти-ми-кроб-ное действие S. boulardii было установлено in vitro и in vivo в отношении возбудителей кишечных инфекций (Cl. difficile, сальмонелл, шигелл, иерсинний), простейших (лямблий и ряда) условно-патогенных микроорганизмов (патогенных кокков, грибов, клебсиелы и др.), способных приводить к развитию СИБР .
Спорообразующие апатогенные антибактериальные средства также могут применяться при СИБР, как альтернатива антибиотикам в случае их непереносимости. К этой группе относятся лекарственные препараты на основе сенной палочки Вacillus subtilis и сходного с ней микроорганизма В. cereus. Споровые микроорганизмы являются для человека транзиторной флорой, поэтому быстро элиминируются из кишечника после прекращения приема. Меха-низм действия этих препаратов обусловлен образованием кислых метаболитов в процессе жизнедеятельности и снижением рН на всем протяжении кишечника, за счет чего ингибируется рост условно-па-тогенной флоры. Кроме то-го, эти средства синтезируют ряд пищеварительных фер-ментов, частично компенсируя снижение собственной ферментной активности кишки при повреждении бактериями и их токсинами. Курс лечения при СИБР составляет 10-14 дней. Более длительный курс нежелателен, т.к. В. cereus способны вырабатывать энтеротоксины, провоцирующие диарею .
Микробные метаболиты
Дополнительным средством, восстанавливающим микрофлору преимущественно тонкой кишки, является микробный метаболит хилак форте . Основными биологически активными компонентами, входящими в состав хилака форте являются короткоцепочечные жирные кислоты (КЖК) и молочная кислота, полученные из сахаролитических и протеолитических представителей нормальной кишечной микрофлоры. Концентрация биологически активных веществ в одной капле препарата соответствует действию соответствующих метаболитов из 1010 бактерий. Механизм действия хилака форте на нормализацию состава и функций микробиоты и на восстановление деятельности кишечника опосредована входящими в него компонентами. Содержащиеся в препарате КЖК обеспечивают слизистые оболочки дополнительной энергией, способствуют регенерации по-врежденных эпителиальных клеток кишечной стенки, улучшают трофику слизистой. Влияние кислых метаболитов (КЖК, молочной кислоты) обеспечивает регуляцию внутрипросветного рН, что приводит к ингибированию роста патогенов и условно-патогенов на всем протяжении кишечника.
Таким образом, тактика лечения ХП с СИБР должна строиться следующим образом:
. адекватная ферментная терапия (Креон 75000 МЕ и более в сутки)
. деконтаминация тонкой кишки: антибактериальная терапия (рифаксимин)
. микробные метаболиты
. нормализация микробиоценоза толстой кишки про- и пребиотиками (при необходимости)
. устранение моторных нарушений - дуоденальной гипертензии, ускоренной пропульсии (при необходимости).


Литература
1. Ардатская М.Д., Минушкин О.Н., Иконников Н.С. «Дисбактериоз кишечника»: понятие, диагностические подходы и пути коррекции. Возможности и преимущества биохимического исследования кала. - Пособие для врачей. - М., 2004.
2. Белоусова Е.А. Синдром избыточного бактериального роста тонкой кишки в свете общей концепции о дисбактериозе кишечника. Взгляд на проблему. //Фарматека, 2009, № 2 с.
3. Бондаренко В.М. Роль условно-патогенных бактерий кишечника в полиорганной патологии человека. М.: Триада, 2007.
4. Бондаренко В.М., Грачева Н.М., Мацулевич Т.В. Дисбактериозы кишечника у взрослых.- М. КМК Scientific Press.-2003.-224 с.
5. Шендеров Б.А. Медицинская микробная экология и фунциональное питание. В 3-х томах. М.: Грантъ, 1998.
6. Коровина Н.А., Захарова И.Н., Костадинова В.н. и др. Пребиотики и пробиотики при нарушениях кишечного микробиоценоза у детей. Пособие для врачей. Медпрактика - М., 2004.
7. Доронин А.Ф., Шендеров Б.А. Функциональное питание. - М.: Грантъ, 2002. - 296 с.
8. Gut Microflora. Digestive Physiology and Pathology. Ed. J-C. Rambaud, J-P. Buts et all. JL Eurontext. Paris. 2006.
9. Парфенов А.И. Энтерология. - М.: Триада, 2002.
10. Approach to the patients with chronic gastrointestinal disorders. Ed. E. Corazziari. MESSAGGI. 2000.
11. Dominguez-Munoz J.E. Pancreatic enzyme therapy for pancreatic exocrine insufficiency. Curr. Gastroenterol Rep. 2007, 9(2): 116-122.
12. Pap А. et al. Влияние терапии Креоном на СИБР у больных с ВСН ПЖ. Abstracts from the 35th European Pancreatic Club Meeting. Pancreatology, 2003; 3: 240.
13. Rifaximin: a Poorly Absorbed Antibiotic. Ed. C. Scarpingato. Karger.2005.
14. Di Stefano M., Сorazza G.R. Treatment of small bowel bacterial overgrowth and related symptoms by Rifaximin. In: Rifaximin: a Poorly Absorbed Antibiotic. Ed. C. Scarpingato. Karger. 2005.
15. Di Stefano M., Malservisi S., Veneto G., Сorazza G.R. Rifaximin versus chlortetracycline in the short term treatment of small intestinal bacterial overgrowth. Aliment Pharmacol Ther 2000; 14: 551-556.
16. Белоусова Е.А. Saccharomyces boulardii (Энтерол) в гастроэнтерологической практике (обзор литературы). //Фарматека, 2006, № 12. с.68-72.
17. Белоусова Е.А., Никитина Н.В., Мишуровская Т.С., Златкина А.Р. Возможности препаратов на основе микробных метаболитов для восстановления кишечной микробиоты //Консилиум, 2005, № 1, с. 9-13.